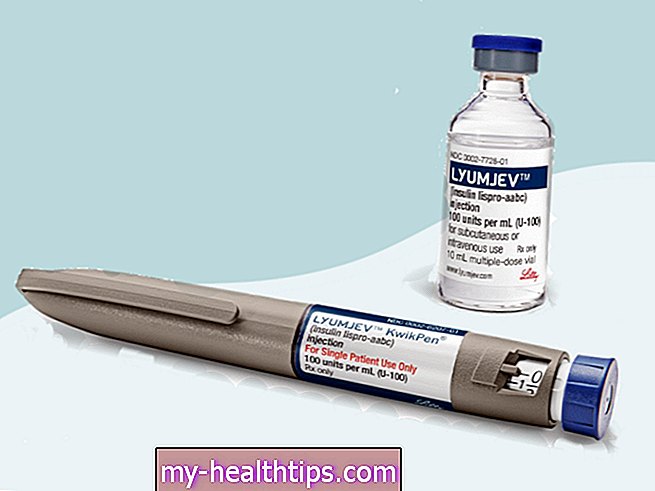
FDA находится в процессе обновления своего окончательного руководства по требуемой точности глюкометров и тест-полосок, слегка изменяя политику, введенную в действие в 2016 году, которая ужесточила проверку этих основных инструментов для управления диабетом.

Хотя некоторые могут задаться вопросом о необходимости или значении этого в то время, когда непрерывные мониторы глюкозы (CGM), кажется, вытесняют традиционные глюкометры, в действительности только небольшой процент ЛОВ (людей с диабетом) используют CGM на сегодняшний день; нереально думать, что традиционные глюкометры и тест-полоски исчезнут в ближайшее время. Это означает, что точность полосы остается критической.
29 ноября FDA выпустило обновленное руководство, в котором изложены стандарты для счетчиков, используемых в клинических условиях, и счетчиков для личного пользования. До февраля 2019 года открыт период общественного обсуждения, после которого агентство рассмотрит отзывы, прежде чем в конечном итоге выпустит официальные окончательные правила.
Те, кто следил за этой проблемой на протяжении многих лет, могут испытывать дежавю из-за подобных обсуждений и чернового варианта руководства, опубликованного в начале 2004 года до того, как окончательные правила были опубликованы в октябре 2016 года. В то время это было огромно, потому что правила точности не изменились. в США с 1990-х годов!
Важно отметить, что новые правила, принятые в 2016 году, касались только новых продуктов и не коснулись счетчиков и полос, уже имеющихся на рынке. Таким образом, хотя эти новые более жесткие требования к точности были положительным изменением, нашему D-сообществу пришлось иметь в виду, что многие менее точные измерители все еще находятся в руках людей с диабетом. Текущие обновления не содержат никаких новых способов контролировать существующие счетчики как таковые, но они предлагают тактику, чтобы «сократить разрыв между показателями до и после выхода на рынок».
«Процедурные изменения» в правилах точности счетчиков
То, что было принято в 2016 году, остается в основном неизменным - это означает, что эти новые изменения, внесенные в ноябре 2018 года, на самом деле не улучшают практическую точность наших счетчиков дома или в клинических условиях.
Вместо этого FDA сообщает нам, что эти новейшие изменения носят в основном «процедурный характер», они касаются того, как производители должны отслеживать свои процессы и трудности, которые они должны пройти, чтобы получить разрешение на выпуск этих измерителей и полосок на рынок. FDA сообщает, что эти изменения были внесены по особому запросу отраслевых игроков, которые посчитали, что документ 2016 года нуждается в разъяснении.
«Изменения в обоих руководствах включали незначительные изменения», - сказала пресс-секретарь FDA Стефани Каккомо. «(Включая) разъяснение того, что спонсоры должны предоставлять обоснования для любых исключений данных при сравнении их методов и оценке пользователей, удаление конкретных примеров модификаций и тестирование критериев выпуска партии, а также добавление сравнений устройства-кандидата в условиях испытаний с устройством-кандидатом в номинальных условиях. для определенных исследований ».
Другими словами, аспекты, которые не имеют большого значения для нас, членов D-сообщества, ежедневно использующих эти продукты в нашем собственном управлении диабетом.
Более раннее руководство, принятое в 2016 году по этим двум классам продуктов, предлагало наиболее значимые изменения:
Для каждого из них стандарты точности требуют, чтобы результаты измерения уровня сахара в крови находились в пределах определенного процента от «эталонного метода» для точности тестирования; им разрешено только быть настолько далекими от сверхточных результатов, которые дает лабораторный тест на глюкозу.
FDA сообщает нам, что они приняли во внимание широкую обратную связь, чтобы найти компромисс, который повысил бы точность, не создавая слишком много препятствий для промышленности.
«Судя по отзывам, полученным от производителей, чрезмерное повышение точности этих полосок приведет к увеличению их затрат при одновременном снижении их доступности для пациентов», - заявила представитель FDA Стефани Каккомо. «Отзывы пациентов показали, что они не хотели снижать удобство использования устройства (из-за увеличения времени тестирования, увеличения объема образца и т. Д.), Чтобы поддерживать постоянные цены на полоски, точность которых была значительно увеличена».
Она добавила, что «это представляет собой значительное улучшение точности по сравнению со счетчиками, продаваемыми на рынке еще 5 лет назад», однако FDA считает, что многие из счетчиков, уже представленных сегодня на рынке, также должны соответствовать этим улучшенным критериям.
Особенности этих критериев заключаются в следующем:
Системы клинического мониторинга уровня глюкозы в крови (BGMS) -
- 95% значений должны находиться в пределах +/- 12% для сахара в крови ниже или выше 75 мг / дл.
- 98% в пределах +/- 15%
Для сравнения, предыдущие правила требовали 15% и 20% точности по всем направлениям. В начале 2014 года FDA предложило ужесточить самые строгие требования до +/- 10%, но производители счетчиков и поставщики медицинских услуг возражали, потому что это могло помешать им производить или получать счетчики по доступной цене. Таким образом, регуляторы собрались в середине на уровне 12%.
Представитель FDA сообщает нам, что причина несоответствия между проектом и окончательной редакцией правил заключается в том, чтобы «сбалансировать клинические потребности каждой группы населения с возможностью производителей производить устройства, отвечающие этим целям».
Вот ссылка на полное 43-страничное руководство FDA для клинических приборов.
Глюкометры для личного пользования -
- 95% в пределах +/- 15% во всем диапазоне измерения
- 99% в пределах +/- 20% во всем диапазоне измерения
Для сравнения, прежние правила требовали 20% точности для большинства диапазонов сахара в крови.
С 2016 г. глюкометры для личного пользования также должны иметь «заметное предупреждение» о том, что их тест-полоски (которые позволяют собирать кровь в «открытой» среде) не предназначены для использования в клинических условиях. Это связано с давней обеспокоенностью как FDA, так и Центров по контролю за заболеваниями (CDC) по поводу риска гепатита B и других заболеваний, передающихся через кровь, и это основная причина, по которой агентство разделило правила на две разные категории.
Вот ссылка на 43-страничный документ FDA для бытовых счетчиков.
Другие требования к новому глюкометру
Производственный процесс: Помимо стандарта точности, FDA также приняло жесткие меры в отношении методологии выпуска партии товара производителями - сбора информации о сайтах производителей и качестве их продукции. Нам сказали, что это достигается за счет «сбора данных и инспекций на местах».
Маркировка: возможно, самое главное, FDA потребовало новой информации о маркировке флаконов с тест-полосками; они должны включать информацию о партии / производстве и описание производительности (данные о точности) на этикетке внешней коробки, чтобы пользователи могли сравнивать один расходомер с другим.
Сторонние тест-полоски: важно, что окончательные правила добавляют положения, специфичные для производителей тест-полосок сторонних производителей, которые в последние годы подверглись критике. Хотя эти полоски часто дешевле, к ним не предъявляются те же требования по точности, что и к счетчикам, особенно когда определенные бренды производятся за границей, и FDA не может инспектировать производственные мощности, как в США. . Теперь правила FDA гласят, что эти производители должны «быть в курсе любых изменений конструкции глюкометра, поскольку такие изменения могут повлиять на совместимость тест-полоски с глюкометром». Это должно быть отражено в документации сторонней компании 510 (k), и FDA также рекомендует предоставить документацию по соглашению между сторонним производителем полос и производителем измерителя.
«Пострыночный надзор» за глюкометрами
В своем недавнем обновлении FDA не включило никаких новых аспектов для проверки счетчиков и полосок после их появления на рынке, за исключением общих положений и политик, которые оно уже имеет для проверок и требований к объектам.
Но агентство осведомлено об этой проблеме и указывает на новые критерии партии тест-полосок как на способ решения проблем после выхода на рынок. FDA рекомендует, чтобы в своих документах 510 (k) производители предоставили описание критериев выпуска партии и краткое изложение схемы отбора проб, которые FDA планирует рассмотреть в рамках разрешения.
«Чтобы сократить разрыв между показателями до и после выхода на рынок, а также различия между партиями тест-полосок, критериев выпуска тестовых партий должно быть достаточно для обеспечения постоянного качества тест-полосок. Это обеспечит большую согласованность между партиями и производителями, а также отпугнет от принятия неверных решений по выпуску продукции после выхода на рынок », - заявила пресс-секретарь Каккомо.
Это была горячая тема в последние годы, что привело к появлению программы наблюдения Общества диабетических технологий, которая сейчас набирает обороты.
Соблюдение является добровольным?
Нет сомнений в том, что новые рекомендации по повышению точности - это хорошо.
Проблема в том, что, хотя медицинские продукты должны быть одобрены Управлением по контролю за продуктами и лекарствами, чтобы поступать на рынок в США, эти «рекомендации» не являются обязательными, а скорее «необязательными», то есть добровольными. Это связано с тем, что в политике FDA говорится, что его руководство «не является юридически обязательным для конкретного курса действий… (но) по-прежнему представляет собой лучший совет агентства по рассматриваемому вопросу на момент их вынесения» - предположительно для защиты агентства от втянуты в судебные процессы.
Но… фу.
Честно говоря, какой в этом смысл, если производители могут просто отказаться от соблюдения этих новых правил? Мы можем только скрестить пальцы, что давление рынка побудит поставщиков соблюдать требования. Несмотря на растущее использование CGM и более автоматизированных D-tech, глюкометры и полоски остаются «хлебом с маслом» в управлении диабетом для масс (так сказать), поэтому обеспечение точности остается важным.


















-and-how-do-i-choose-one.jpg)